ГЛАВНЫЕ НОВОСТИ
События

Қазақстандық «Нобел Алматы фармацевтикалық фабрикасы» АҚ Түркияның Дәрілік заттар және медициналық бұйымдар жөніндегі агенттігінің (TİTCK) инспекциясынан сәтті өтіп, сала көшбасшысы мәртебесін кезекті рет дәлелдеді.
Түрік реттеуші органынан GMP сертификатын алу - бұл жай ғана ресмилік емес. Бұл «Нобел АФФ» кәсіпорнындағы өндірістік процестердің Тиісті өндірістік практиканың (GMP) қатаң халықаралық стандарттарына сәйкестігін ресми түрде тану болып табылады. Тұтынушы үшін бұл - конвейерден шыққан әрбір препараттың сапа, қауіпсіздік және тиімділік бойынша жоғары көрсеткіштерін тұрақты сақтайтынының басты кепілі.
Кәсіпорын үшін бұл нәтиже экспорттық бағытты дамыту және халықаралық жеткізу тізбегіне интеграциялану тұрғысынан стратегиялық маңызға ие. TİTCK тарапынан танылу өнімді Түркия нарығында тіркеу және шығару үшін қосымша мүмкіндіктер туғызады, сондай-ақ шетелдік реттеушілер мен іскер серіктестердің сенімін нығайтады. Осылайша, бұл жетістік - қазақстандық технологиялар мен тәжірибенің бүгінде ең жоғары халықаралық деңгейде мойындалғанының нақты дәлелі.
Салалық контексте жетекші шетелдік реттеушілерден GMP сертификаттарын алу бәсекеге қабілеттіліктің негізгі факторы болып табылады. Түріктің TİTCK реттеушісі PIC/S ұйымының толық құқықты мүшесі және ICH қатысушысы болғандықтан, оның инспекциялары Еуропалық дәрі-дәрмек агенттігінің (EMA) талаптарымен толық үйлестірілген. Бұл «Нобел АФФ» өндірістік стандарттарының әлемдік үздік практикалармен деңгейлес екенін және жаһандық деңгейде танылатынын растайды.
«Нобел АФФ» АҚ жүріп өткен жолы — бұл қазақстандық бизнестің өршіл мақсаттар қойып, оған жете білуінің жарқын үлгісі. Жаһандық GMP стандарттарын дәйекті түрде енгізу отандық фармацевтиканың реттеушілік кемелдіктің жаңа деңгейіне шыққанын дәлелдейді. Бүгінде біз жай ғана дәрі-дәрмек шығарып қоймай, әрбір қазақстандық мақтан тұтатын заманауи, экспортқа бағытталған индустрия құрып жатырмыз. Бұл - еліміздің әлемдік денсаулық сақтау картасында мойындалған интеллектуалды және өндірістік орталыққа айналуына жасалған нық қадам.
Компания туралы
«Нобел Алматы Фармацевтикалық Фабрикасы» АҚ - Қазақстандағы жетекші фармацевтикалық өндірушілердің бірі. Кәсіпорын 2002 жылы құрылған. Компания аурулардың кең спектрін емдеуге арналған рецептілік және рецептісіз дәрілік заттардың бай ассортиментін шығарады және Молдова, Өзбекстан, Қырғызстан мен Моңғолияға экспортты жүзеге асырады. Кәсіпорын алаңында инновациялық дәрілік препараттардың келісімшарттық өндірісі жобалары іске асырылуда, оның ішінде Abbott Products Operations AG, F. Hoffmann-La Roche Ltd және AstraZeneca сияқты халықаралық фармацевтикалық корпорациялармен ынтымақтастық орнатылған.
Осылайша, «Нобел АФФ» АҚ тек өндіріс алаңы ретінде ғана емес, сонымен бірге инновациялық технологияларды енгізуді, жергілікті өндірісті дамытуды және пациенттердің заманауи емдеу әдістеріне қолжетімділігін қамтамасыз ететін Қазақстанның фармацевтика саласын трансформациялаудың негізгі қатысушысы ретінде әрекет етеді.

11–12 июня 2026 года в Ташкенте состоится V Международный фармацевтический форум Узбекистана - одна из ключевых профессиональных площадок для стратегического диалога и развития партнёрств в фармацевтической отрасли Центральной Азии.
Форум ежегодно объединяет более 250 делегатов из более чем 23 стран, включая представителей государственных и регуляторных органов,
международных и региональных фармацевтических компаний, дистрибуторов, инвесторов и отраслевых экспертов. За годы проведения форум зарекомендовал себя как устоявшаяся профессиональная платформа, в рамках которой формируются практические решения, заключаются партнёрства и инициируются инвестиционные проекты.
Повестка форума 2026 года включает:
• стратегию развития фармацевтического рынка Узбекистана до 2030 года
• локализацию и контрактное производство
• лекарственное страхование и государственные закупки
• аналитику рынка и ценообразование
• регистрацию и регуляторное сближение с международными стандартами
• фармацевтическую дистрибуцию и коммерческие стратегии
Мероприятие проходит при официальной поддержке Министерства здравоохранения, Агентства по развитию фармацевтической отрасли и Ассоциации представительств иностранных фармацевтических компаний в Узбекистане, а также других профильных государственных органов Республики Узбекистан.
Место проведения:
InterContinental Tashkent г. Ташкент, ул. Шахрисабз, 2
Регистрация и подробная информация:
www.uzpharmforum.com
+998 94 094 88 88

Казахстанское предприятие АО «Нобел Алматинская фармацевтическая фабрика» в очередной раз подтвердила статус лидера отрасли, успешно пройдя инспекцию Турецкого агентства по лекарственным средствам и медицинским изделиям (TİTCK).
Получение сертификата GMP от турецкого регуляторного органа - это не просто формальность. Это официальное признание того, что производственные процессы «Нобел АФФ» соответствуют строгим международным стандартам Надлежащей производственной практики (GMP). Для потребителя это главный гарант того, что каждый препарат, сошедший с конвейера, стабильно сохраняет высокие показатели качества, безопасности и эффективности.
Для предприятия данный результат имеет стратегическое значение в точки зрения развития экспортного направления и интеграции в международные цепочки поставок. Признание со стороны TİTCK создаёт дополнительные возможности для регистрации и вывода продукции на рынок Турции, а также усиливает доверие со стороны зарубежных регуляторов и деловых партнёров. Таким образом, данный результат - это реальное доказательство того, что казахстанские технологии и опыт сегодня признаны на самом высоком международном уровне.
В отраслевом контексте получение GMP-сертификатов от ведущих иностранных регуляторов является ключевым фактором конкурентоспособности. Поскольку турецкий регулятор TİTCK является полноправным членом PIC/S и участником ICH, его инспекции полностью гармонизированы с требованиями European Medicines Agency (EMA). Это подтверждает, что производственные стандарты «Нобел АФФ» сопоставимы с лучшими мировыми практиками и признаются на глобальном уровне.
Путь АО «Нобел АФФ» - это пример того, как казахстанский бизнес ставит амбициозные цели и достигает их. Последовательное внедрение глобальных стандартов GMP доказывает: отечественная фармацевтика вышла на новый уровень регуляторной зрелости. Сегодня мы не просто производим лекарства, мы строим современную, экспортно-ориентированную индустрию, которой может гордиться каждый казахстанец. Это уверенный шаг к тому, чтобы наша страна стала признанным интеллектуальным и производственным центром на мировой карте здравоохранения
О компании
АО «Нобел Алматинская Фармацевтическая Фабрика» является одним из ведущих фармацевтических производителей Казахстана. Предприятие основано в 2002 году.
Компания выпускает широкий ассортимент рецептурных и безрецептурных лекарственных средств, применяемых в терапии широчайшего спектра заболеваний, и осуществляет экспорт в Молдову, Узбекистан, Кыргызстан и Монголию. На площадке предприятия реализуются проекты контрактного производства инновационных лекарственных препаратов, включая сотрудничество с международными фармацевтическими корпорациями Abbott Products Operations AG, F. Hoffmann-La Roche Ltd и AstraZeneca.
Таким образом, АО «Нобел АФФ» выступает не только как производственная площадка, но и как ключевой участник трансформации фармацевтической отрасли Казахстана, обеспечивающий внедрение инновационных технологий, развитие локального производства и расширение доступа пациентов к современным методам лечения.
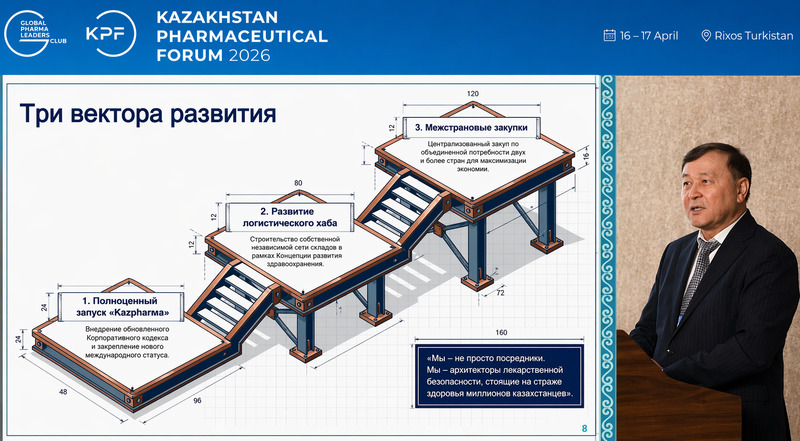
16–17 апреля 2026 года в Туркестане прошел Казахстанский фармацевтический форум - одна из ключевых экспертных площадок, объединяющая представителей государственных органов, международных и отечественных фармацевтических компаний, а также профильных организаций для выработки согласованных решений в сфере лекарственного обеспечения.
Участники отрасли обсудили трансформацию государственных закупок, развитие локального производства и расширение доступа к инновационным препаратам.
В работе форума приняла участие расширенная делегация ТОО «СК-Фармация» во главе с председателем правления Нурлыбеком Асылбековым. В рамках форума он представил стратегическое видение развития отрасли:
«Обеспечение лекарственной безопасности - это не только задача системы здравоохранения, но и важнейший элемент национального суверенитета. Сегодня «СК-Фармация» трансформируется из оператора логистики в стратегический интегратор устойчивой фармацевтической системы. За счёт централизации закупок, цифровизации процессов и поддержки отечественного производства мы формируем систему, способную эффективно отвечать на глобальные вызовы.
Мы уже достигли значимых результатов: ежегодная экономия бюджетных средств в миллиарды тенге позволяет расширять доступ к бесплатным лекарствам; сформирован неснижаемый запас препаратов, обеспечивающий бесперебойность поставок; внедряется распределённая логистическая инфраструктура, охватывающая все регионы страны.
Наш приоритет - развитие отечественного производства и переход от импортозамещения к технологическому суверенитету. Через долгосрочные контракты мы создаём условия для локализации международных фармацевтических компаний и трансфера технологий.
Важнейшим направлением остаётся цифровизация: внедрение систем прослеживаемости и предиктивного планирования повышает прозрачность цепочки поставок и обеспечивает контроль качества препаратов для каждого пациента.
В перспективе мы видим развитие межгосударственных закупок, формирование регионального логистического хаба и переход к новому этапу развития под брендом Kazpharma - как символа надёжности и конкурентоспособности Казахстана на глобальном фармацевтическом рынке».
Итоги форума подтверждают готовность всех участников отрасли к дальнейшему укреплению взаимодействия и внедрению современных управленческих и регуляторных решений. Консолидация усилий государства, профессионального сообщества, бизнеса и пациентских организаций создает прочную основу для формирования эффективной, прозрачной и устойчивой системы лекарственного обеспечения, ориентированной на главную ценность - здоровье и благополучие граждан Республики Казахстан.

16–17 апреля 2026 года в Туркестане начал работу Казахстанский фармацевтический форум. В рамках пленарной сессии председатель Комитета медицинского и фармацевтического контроля Министерства здравоохранения Республики Казахстан Бауыржан Джусипов обозначил основные направления государственной политики в сфере регулирования фармацевтического рынка.
Как отметил спикер, ключевыми приоритетами остаются обеспечение доступности безопасных и качественных лекарственных средств и медицинских изделий, формирование сбалансированной справедливой системы ценообразования, усиление контроля качества, а также цифровизация отрасли.
В настоящее время в Казахстане зарегистрировано более 20 тыс. лекарственных средств и медицинских изделий, при этом свыше 15% продукции производится отечественными компаниями.
Одним из приоритетных направлений является упрощение процедур регистрации. С 2025 года реализуется пилотный проект по внедрению композитной государственной услуги по принципу «единого окна», предусматривающий оптимизацию экспертизы и сокращение сроков регистрации. Для лекарственных средств, одобренных в странах с развитой системой регулирования обращения лекарственных средств, будет применяться ускоренная процедура - до 15 рабочих дней. В рамках данной модели предусмотрено параллельное формирование предельных цен и включение препаратов в Национальный лекарственный формуляр. В перспективе планируется расширение перечня стран с развитой регуляторной системой, а также внедрение механизма регистрации по инициативе государства для оперативного обеспечения населения жизненно-важными препаратами.
Соответствующие нормы одобрены на пленарном заседании в рамках законопроекта по вопросам науки: документ принят Мажилисом Парламента РК и направлен на рассмотрение в Сенат Парламента РК.
Вторым направлением обозначено усиление системы контроля качества и безопасности лекарственных средств. В стране реализуется комплексный подход, включающий развитие фармаконадзора, оценку безопасности при ввозе и применение риск-ориентированной модели отбора препаратов с рынка для контроля качества.
В части дальнейшего развития фармаконадзора предусмотрено внедрение интегрированной информационной системы, синхронизированной с медицинскими информационными системами и международными базами данных. Это позволит повысить эффективность мониторинга безопасности лекарственных средств на всех этапах обращения. Дополнительно будет усилен контроль качества незарегистрированных препаратов, ввозимых по разовым разрешениям.
В рамках повышения доступности лекарственных средств реализуется комплекс мер, включая освобождение от НДС препаратов, предоставляемых в системе гарантированного объёма бесплатной медицинской помощи и обязательного социального медицинского страхования. Налоговые преференции распространяются более чем на 3000 наименований, из которых порядка 1200 применяются для лечения орфанных и социально-значимых заболеваний. Освобождение действует на всех этапах обращения - от оптового звена до розничной реализации.
Параллельно осуществляется мониторинг цен в розничном сегменте с использованием цифровых инструментов. В системе маркировки и прослеживаемости товаров внедрён функционал контроля предельных цен, позволяющий анализировать фактическую стоимость лекарственных средств в аптечных организациях. По итогам первого квартала 2026 года, при анализе около 2000 наименований установлено, что более 50% препаратов сохраняют стабильный ценовой уровень, что указывает на относительную устойчивость ценовой ситуации на рынке.
В целях формирования конкурентной среды и повышения доступности лекарственных средств реализуется поэтапное дерегулирование цен в оптовом и розничном сегментах. С 2023 года выведены из регулирования цен 1800 безрецептурных препаратов. Следующим этапом, начиная с апреля текущего года, предусматривается вывод из ценового регулирования лекарственных средств стоимостью до одного МРП. Соответствующий приказ Министерства здравоохранения подписан и направлен на государственную регистрацию. Ожидается, что данная мера затронет свыше 2500 наименований.
Как ключевой инструмент повышения эффективности системы лекарственного обеспечения рассматривается цифровизация. Министерством здравоохранения РК реализуется комплекс проектов, направленных на внедрение электронного выписывания и учёта лекарственных препаратов. В медицинских информационных системах функционирует механизм электронных рецептов, интегрированный с системой лекарственного обеспечения, что позволило сократить время оформления назначений вдвое.
Дополнительно электронные рецепты реализованы в рамках проекта «Социальный кошелёк»: на текущий момент обеспечено более 10 млн рецептов в 700 медицинских организациях.
В перспективе предусмотрено внедрение технологий искусственного интеллекта для прогнозирования потребностей и объёмов поставок лекарственных средств, а также для выявления неэффективных назначений и повышения прозрачности системы.
В системе маркировки товаров планируется запуск интеллектуального консультанта, который обеспечит автоматизированную поддержку участников рынка по вопросам маркировки, требований законодательства и правил обращения продукции.
В заключении Бауыржан Джусипов отметил готовность к открытому взаимодействию с отраслевым сообществом в целях реализации инициатив, направленных на повышение устойчивости системы здравоохранения и обеспечение равного доступа населения к качественным, безопасным и эффективным лекарственным средствам и медицинским изделиям.

1–2 апреля 2026 года в Москве состоялась Международная практическая конференция «Регистрация лекарственных средств по правилам ЕАЭС», организованная конгресс-оператором BRAVO BUSINESS FORUMS. В рамках форума был озвучен доклад заместителя отдела координации работ в сфере обращения лекарственных средств и медицинских изделий Департамента технического регулирования и аккредитации Евразийской экономической комиссии А.М. Кравчук, в котором были представлены ключевые изменения в регулировании обращения лекарств в ЕАЭС, а также основные направления развития нормативной базы на 2026 год.
Анна Михайловна представила статитику регистрации лекарственных средств по правилам ЕАЭС. Так, по состоянию на апрель 2026 года, подано 53 807 заявлений по правилам Союза, выдано более 15 262 регистрационных удостоверений. Параллельно существенно активизировалась инспекционная деятельность - выдано 3 482 GMP-сертификата при 5 349 заявках на инспектирование.
В числе основных направлений развития регулирования сферы обращения лекарственных средств ЕАЭС в 2025 году докладчик назвала уточненения требований к медицинским изделиям, помещаемым в упаковку лекарственных препаратов. Кроме того, установлены правовые основания для обращения продукции, которая не реализуется на рынке ЕАЭС отдельно, но поставляется в составе лекарственного препарата, что позволило снять ряд регуляторных ограничений.
Существенные изменения затронули процедуры внесения изменений в регистрационное досье. Пересмотрены как административные подходы, так и классификация изменений, оптимизированы процедуры приведения в соответствие, а также скорректированы сроки их выполнения.
Принята новая редакция требований к общей характеристике лекарственного препарата, а также объединены документы, регулирующие определение категории отпуска (рецептурный/безрецептурный). Кроме того, актуализированы требования к маркировке лекарственных средств.
В сфере исследований лекарственных средств пересмотрены ключевые нормативные акты, включая правила проведения исследований биоэквивалентности для немодифицированных лекарственных форм и форм для местного применения. Произведена корректировка выбора референтного препарата, процедуры биовейвера на основе БСК.
Значительное внимание уделяется развитию Фармакопеи ЕАЭС. В 2025 году завершена подготовка третьей ее части, при этом четвёртая часть находится на завершающем этапе технической доработки. Параллельно подготовлены методические рекомендации по разработке фармакопейных статей. Несмотря на то, что данный документ не носит обязательного характера, он отражает согласованную позицию регуляторов стран ЕАЭС и может использоваться производителями при подготовке нормативной документации по качеству.
Завершена подготовка правил инспектирования для всех надлежащих практик, включая правила надлежащей лабораторной практики. Существенным шагом стала и актуализация правил GMP, новая редакция приведена в соответствие с международным стандартом ICH E6(R2).
В 2026 году регуляторная повестка ЕАЭС в сфере обращения лекарственных средств будет сосредоточена на актуализации ключевых нормативных документов и развитии новых направлений регулирования. Как следует из представленной информации, в высокой степени готовности находится ряд документов, которые уже прошли или завершают этап общественного обсуждения и готовятся к рассмотрению Коллегией или Советом ЕЭК.
Одним из центральных направлений станет актуализация правил GMP, в частности, существенным нововведением станет подготовка нового раздела, который будет посвящён требованиям к высокотехнологичным лекарственным препаратам, что отражает растущую значимость данной категории продуктов для рынка ЕАЭС.
В рамках развития надлежащей дистрибьюторской практики (GDP) разрабатывается руководство по проведению температурного картирования. Необходимость такого документа обусловлена частыми вопросами, возникающими в ходе инспекций складских помещений, в частности в части оформления и обоснования температурных режимов. Предполагается, что новое руководство позволит унифицировать подходы и обеспечить единое понимание требований со стороны регуляторов всех стран ЕАЭС.
В блоке, связанном с проведением исследований, подготовлен проект руководства по определению объёма лабораторных испытаний. Документ направлен на актуализацию отдельных положений с учётом ранее внесённых изменений в правила проведения исследований биоэквивалентности и призван обеспечить согласованность требований.
Дополнительно актуализируются документы, относящиеся к GMP, в частности руководство по проектированию, эксплуатации, квалификации и техническому обслуживанию систем отопления, вентиляции и кондиционирования воздуха (HVAC), применяемых при производстве нестерильных лекарственных средств. Новая редакция учитывает как международные требования, так и накопленный опыт проведения инспекций.
В числе ближайших планов - принятие руководства по микробиологическому мониторингу, которое уже прошло общественное обсуждение и, как ожидается, будет утверждено в конце 2026 - начале 2027 года.
Значительный объём работы продолжается в рамках формирования фармакопеи ЕАЭС. Фармакопейным комитетом завершена разработка основного блока статей для четвёртой части первого тома. В настоящее время проводится научное редактирование, а принятие документа ожидается в третьем–четвёртом квартале 2026 года.
Параллельно ведётся разработка дополнительных глав к правилам проведения исследований биологических лекарственных средств. В центре внимания - вопросы биосимиляров, внедрение риск-ориентированного подхода к оценке высокотехнологичных препаратов, а также требования к доклиническим и клиническим исследованиям геннотерапевтических лекарственных средств. Эти документы находятся на высокой стадии готовности и планируются к принятию в текущем году.
Одновременно Комиссия продолжает работу над руководством по управлению жизненным циклом лекарственных препаратов, гармонизированное с ICH Q12. Документ будет регулировать подходы к управлению пострегистрационными изменениями и станет важным инструментом для систематизации процессов, связанных с качеством лекарственных средств.
Важным направлением является и разработка руководств по клинической разработке лекарственных препаратов. Уже одобрены документы, посвящённые терапии болезни Альцгеймера и сердечной недостаточности. В стадии обсуждения находится руководство по онкологическим заболеваниям, разработка которого только начинается.
Одной из новых инициатив является разработка подходов к регулированию препаратов крови. В частности, рассматривается возможность внедрения мастер-файла плазмы крови с последующей выдачей соответствующего сертификата. Предполагается, что данный инструмент будет концептуально схож с мастер-файлом на фармацевтическую субстанцию. В настоящее время проект находится на стадии формирования концепции, и окончательные параметры регулирования ещё не определены.
Параллельно обсуждаются изменения, касающиеся требований GMP в составе регистрационного досье. Данный блок находится на этапе активного обсуждения, и конкретные регуляторные решения, которые могут повлиять на процедуры регистрации и инспектирования, пока не сформированы.
Существенное внимание уделяется вопросам контроля качества лекарственных средств. Планируется актуализация требований к аналитическим методикам, включая их разработку и валидацию. Также предусмотрен пересмотр требований к исследованиям стабильности, а также к контролю остаточных растворителей и примесей. Эти изменения направлены на приведение нормативной базы в соответствие с современными научными и технологическими подходами.
Продолжается развитие нормативной базы в части проведения исследований биоэквивалентности, включая уточнение отдельных положений и расширение методологической базы. Важным направлением остаётся формирование фармакопеи ЕАЭС. В настоящее время ведётся работа по подготовке второго тома, который будет включать частные фармакопейные статьи на вспомогательные вещества и активные фармацевтические субстанции. Уже одобрена первая статья, что свидетельствует о переходе к новому этапу развития фармакопеи, предусматривающему более детализированное регулирование требований к качеству конкретных веществ.
Отдельный приоритет - разработка руководств по проведению клинических исследований в особых группах населения. Речь идёт о педиатрической популяции, а также о беременных и лактирующих женщинах.
В рамках развития регулирования биологических лекарственных средств продолжается актуализация соответствующих правил. Особое внимание уделяется расширению применения концепции биосимиляров, а также разработке специализированных требований к вакцинам, иммуноглобулинам и клеточным субстратам.
Планируется актуализация требований к электронному формату регистрационного досье и заявлений, что связано с необходимостью их приведения в соответствие с последними изменениями правил регистрации. Также рассматриваются изменения в правила надлежащей дистрибьюторской практики, в первую очередь в части обращения активных фармацевтических субстанций.
Отдельным направлением становится развитие подходов к использованию данных реальной клинической практики (real-world data), а также внедрение технологий искусственного интеллекта в регуляторные процессы. В настоящее время эти вопросы находятся на стадии обсуждения, формируются базовые подходы к их применению.
Таким образом, регуляторная политика ЕАЭС в 2026 году направлена на последовательную гармонизацию нормативной базы с международными подходами, повышение прозрачности требований и развитие специализированных инструментов регулирования, охватывающих весь жизненный цикл лекарственного препарата - от разработки до пострегистрационного сопровождения.

7 апреля 2026 года в Алматы в рамках Фармацевтического форума «Современное состояние фармацевтической отрасли Республики Казахстан: вектор развития» был подписан Меморандум о сотрудничестве между Министерством здравоохранения Республики Казахстан и Объединением юридических лиц в форме «Ассоциации поддержки и развития фармацевтической деятельности Республики Казахстан».
Документ подписали вице-министр здравоохранения Республики Казахстан Тимур Муратов и президент Ассоциации Марина Дурманова. Подписание меморандума стало одним из ключевых практических итогов форума, объединившего представителей государственных органов, экспертного сообщества и бизнеса.
Целью соглашения определено развитие фармацевтической отрасли Казахстана через усиление взаимодействия между регулятором и профессиональным сообществом. Согласно документу, стороны намерены выстраивать сотрудничество по широкому спектру направлений. В их числе - совершенствование системы лекарственного обеспечения и предоставления фармацевтических услуг населению, развитие механизмов ценообразования на лекарственные средства и медицинские изделия, а также усиление контроля за качеством, безопасностью и эффективностью продукции.
Отдельное внимание будет уделено развитию нормативно-правовой базы лекарственной политики и формированию стратегических документов государственного регулирования, направленных на повышение доступности лекарственных средств и развитие фармацевтической и медицинской промышленности.
В рамках меморандума предусмотрено взаимодействие по вопросам лицензирования фармацевтической деятельности, определению приоритетных направлений научных исследований, а также развитию кадрового потенциала отрасли.

В рамках Фармацевтического форума «Современное состояние фармацевтической отрасли Республики Казахстан: вектор развития» состоялась панельная сессия «Цифровая маркировка и прослеживаемость лекарственных средств, медицинских изделий и биологически активных добавок». Евгений Землянкин, генеральный директор ТОО «Эмити Интернешнл», выделил ключевые достижения и проблемные зоны внедряемой системы.
Бизнес признает, что концептуально система маркировки обоснована. Государство получило мощный инструмент для контроля товарных потоков, что особенно критично в следующих аспектах:
• Бюджетные закупки: мониторинг поставок в лечебно-профилактические учреждения (ЛПУ).
• Пресечение нарушений: возможность отслеживать незаконный переток продукции, закупленной в рамках ГОБМП и ОСМС, в частные аптеки.
Скептицизм коммерческого сегмента
Для частного рынка дополнительная ценность системы остается под вопросом:
• Достаточность данных: аналитические агентства уже предоставляют высокую прозрачность рынка, позволяя отслеживать движение позиций до уровня конкретной аптеки, не раскрывая коммерческую тайну.
• Экономическая нагрузка: в системе участвуют около 12 тысяч субъектов (производители, дистрибьюторы, аптеки, медицинские учреждения).
• Кадровый вопрос: крупные предприятия вынуждены создавать целые департаменты для обеспечения маркировки, в то время как в малых аптеках эта нагрузка дополнительно ложится на плечи минимум одного сотрудника.
Финансовые последствия для бюджета
Внедрение системы сопровождается значительными операционными расходами, которые напрямую влияют на налогооблагаемую базу.
При условно-минимальной оценке затрат на уровне 100 тыс. тенге на одного специалиста, совокупные расходы участников рынка на сопровождение процесса маркировки составляют не менее 1,2 млрд тенге ежемесячно. В результате потенциальные выпадающие доходы бюджета по КПН могут составлять 240 млн тенге ежемесячно. «С точки зрения бизнеса, если государство требует - значит, это нужно делать. Но с точки зрения эффективности вложенных инвестиций - отдача пока близка к нулю», - резюмировал Евгений Землянкин.
Новости

В аптеках Казахстана выявлена реализация 4114 препаратов, закупленных для ГОБМП

Всемирный день гемофилии: диагностика - чтобы быть в контроле, в движении, вовремя

В Казахстане ускорят вывод лекарств на рынок: поправки приняты во втором чтении
Минздрав Казахстана: цены на лекарства снизились по результатам мониторинга
Кыргызстан внедряет ускоренную и упрощенную модель регистрации лекарств
Узбекистан готовит запуск онлайн-продажи лекарственных средств через маркетплейсы
Указание ИИН пациента планируют сделать обязательным в чеках на медуслуги и лекарства

Недоступность стоматологической помощи связана повышенной частотой ССЗ и деменции
В РК расширяют контроль незаконной медицинской деятельностью и оборотом лекарств
Статьи

Әлемдік деңгейдегі Қазақстандық сапа: «Нобел АФФ» ...

Казахстанское качество на мировом уровне: «Нобел А...
ТОО «СК-Фармация» перейдет к новому этапу развития...

Бауыржан Джусипов обозначил основные направления в...

Регулирование обращения лекарств в ЕАЭС: итоги 202...

Между Министерством здравоохранения РК и АПРФД РК ...

Маркировка и налоги: как прослеживаемость влияет н...

Казахстан - первая страна в ЦА, получившая признан...

Лекарственное обеспечение в Казахстане: новые регу...

30 лет АПРФД РК: от становления рынка к формирован...
Аналитика

Prindex & Pharma-Q — ориентиры в новых реалиях фар...

Фармацевтический рынок Казахстана — итоги 2025: кл...

Фармацевтический рынок Таджикистана: структура, др...

За последний год продажи витаминов в Казахстане в...

Как увеличились цены на платные медицинские услуги...
Аптечный рынок Казахстана: ключевые изменения, выз...

Proxima Research: сетевые аптеки в Казахстане акку...

Промоция и назначения на фармацевтическом рынке Ка...

ОБЗОР ФАРМАЦЕВТИЧЕСКОГО РЫНКА РЕСПУБЛИКИ КАЗАХСТАН...























